Значение гипофиза для роста и развития ребенка
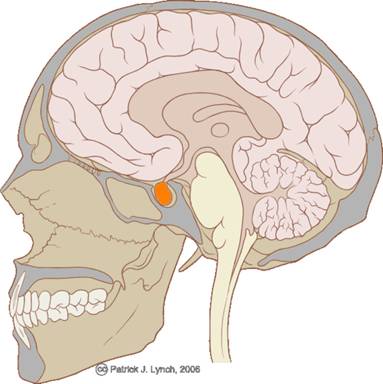
 Гипо́физ — мозговой придаток в форме округлого образования, расположенного на нижней поверхности головного мозга в костном кармане, называемом турецким седлом, вырабатывает гормоны, влияющие на рост, обмен веществ и репродуктивную функцию. Является центральным органом эндокринной системы.
Гипо́физ — мозговой придаток в форме округлого образования, расположенного на нижней поверхности головного мозга в костном кармане, называемом турецким седлом, вырабатывает гормоны, влияющие на рост, обмен веществ и репродуктивную функцию. Является центральным органом эндокринной системы.
Вес гипофиза составляет около 0,5—0,6 г., он состоит из двух крупных различных по происхождению и структуре долей: передней — аденогипофиза (составляет 70—80 % массы органа) и задней — нейрогипофиза. Вместе с нейросекреторными ядрами гипоталамуса гипофиз образует гипоталамо-гипофизарную систему, контролирующую деятельность периферических эндокринных желёз.
Закладка гипофиза происходит на 4—5 неделе эмбриогенеза. Передняя доля гипофиза развивается из эпителиального выпячивания дорсальной стенки ротовой бухты в виде пальцевидного выроста (кармана Ратке), направляющегося к основанию головного мозга, в области III желудочка, где встречается с будущей задней долей гипофиза, которая развивается позднее передней из отростка воронки промежуточного мозга.
Гипофиз тесным образом соединен с гипоталамусом — отделом мозга, играющим важнейшую роль в регуляции многих процессов в организме, в том числе в поддержании постоянства внутренней среды, терморегуляции, деятельности внутренних органов. Гипоталамус содержит как нервные клетки, участвующие в деятельности вегетативной нервной системы (регулирующей многие функции внутренних органов), так и секреторные клетки, которые вырабатывают так называемые рилизинг-гормоны. Эти гормоны призваны оказывать строго специфическое воздействие на гипофиз, побуждая его повышать или снижать выработку тех или иных гормонов в зависимости от потребностей организма.
Гипофиз ребенка при рождении имеет массу около 0,12 г. Его рост и функциональное развитие продолжается до 20-летнего возраста. А поскольку гипофиз является регулятором деятельности всех остальных желез внутренней секреции, то его функциональная незрелость обусловливает некоторую нестабильность всей эндокринной системы ребенка. Одним из гормонов выделяемых гипофизом является соматотропин, который называют гормоном роста за то, что у детей и подростков, а также молодых людей с ещё не закрывшимися зонами роста в костях он вызывает выраженное ускорение линейного (в длину) роста, в основном за счет роста длинных трубчатых костей конечностей. Соматотропин оказывает мощное анаболическое и анти-катаболическое действие, усиливает синтез белка и тормозит его распад, а также способствует снижению отложения подкожного жира, усилению сгорания жира и увеличению соотношения мышечной массы к жировой. Кроме того, соматотропин принимает участие в регуляции углеводного обмена — он вызывает выраженное повышение уровня глюкозы в крови и является одним из антагонистов инсулина по действию на углеводный обмен. Описано также его действие на островковые клетки поджелудочной железы, иммуностимулирующий эффект, усиление поглощения кальция костной тканью и др. Многие эффекты гормон роста вызывает непосредственно, но значительная часть его эффектов опосредуется инсулиноподобными факторами роста, который вырабатывается под действием гормона роста в печени и стимулирует рост большинства внутренних органов.
Получить выполненную работу или консультацию специалиста по вашему
учебному проекту
Узнать стоимость
Источник
Мы продолжаем обсуждение вопросов, касающихся работы гипофиза. Мы уже определились, что выделение гормонов гипофиза будет находиться под действием разного рода регулирующих сигналов. Работа стимулируется выделением особых рилизинг-гормонов. Это гормоны гипоталамуса, которые регулируют секрецию гормонов в гипофизе.
Группа рилизинг-гормонов производится в области особых клеток в головном мозге, в особой гипоталамической области, которая очень тесно связана с гипофизом. Также, секреция гормонов в гипофизе по типу ТТГ или АКТГ, с другой стороны, регулируется по принципу обратной связи. Подавляется при повышении уровня гормонов и стимулируется при понижении концентрации гормонов. При этом за счет такой слаженной работы организма не проявляется никаких симптомов нарушений в работе гипофиза. Кроме того, работа гипофиза контролируется гипоталамусом и взаимодействует с другими видами гормонов. К примеру, воздействие гормона роста будет подавляться выделением вещества – соматостатина, который будет производиться в гипоталамусе, в области поджелудочной железы и в области особых эндокринных клеток в области многих других органов. Также происходит и регуляция продукции пролактина, она подавляется за счет дофамина, особого гормона из группы гормонов адреналина. Важно понимать, что гипофиз может представлять собой крайне сложный железистый орган, при его болезнях или разрушении могут страдать функции многих эндокринных желез.
Расстройства работы гипофиза.
Есть целый ряд заболеваний, при которых происходят нарушения в работе гипофиза, и важно своевременно их распознавать. Особенно явными и выраженными проблемами гипофиза являются нарушения роста. Обычно нарушения в росте могут наблюдаться наследственные особенности, и в целом дети повторяют основные ростовые особенности своих родителей. Также возникают генетические дефекты в росте костей. В таких случаях замедления в росте происходят очень непропорционально, при этом происходит укорочение костей в области конечностей. Также происходят проблемы вследствие нарушений в питании или в результате общих тяжелых соматических заболеваний. Мы с вами подробнее поговорим об особенностях нарушений роста в результате поражений в гипофизе.
Особенно это важно для детей. Чтобы выявить нарушения роста, важно регулярно составлять ростовую и весовую кривые ребенка в карте его развития на стандартном бланке его росто-весовых показателей. Кривая роста ребенка в нормальных условиях должна проходить параллельно стандартной кривой. Это не зависит от того, находятся ли они в области верхней, нижней или средней зоны. О нарушениях в росте можно у ребенка говорить тогда, когда кривая ростовых показателей начинает отклоняться от стандартной вверх или вниз, если она пересекает стандартные кривые. Также для родителей важно будет определить вероятный окончательный рост своего ребенка, и сделать это относительно несложно. Поскольку рост во многом зависит от разного рода наследственных факторов, его очень просто можно подсчитать по особой формуле. Нужно сложить рост отца и рост матери, разделив их на два и получив среднее значение. К этому среднему значению для мальчика прибавляют 6-7 см, для девочки отнимают 6-7 см. обычно ошибки по данному прогнозу не превышают отклонений 8 см в ту или иную сторону в зависимости от того, какие внешние факторы и условия среды также влияют на рост.
При обращении к врачу по поводу изменений в росте, он определяет обычно так называемый костный возраст, который основывается на рентгенограммах и специальных таблицах, в которых указаны возрастные показатели. Обычно ускорения в росте будет редко связано с нарушениями в функциях гипофиза. При развитии гипофизарного гигантизма, который возникает обычно у юношей, имеется свойство повышения продукции гормона роста в результате формирования опухоли самой железы. Иногда развитие гигантизма может также сочетаться с развитием акромегалии – ускоренным и непропорциональным ростом в области костей лицевого черепа, конечностей, особенно кистей рук и стоп. Зачастую, резкое ускорение роста тела может наблюдаться при наличии семейной высокорослости. У таких детей имеются вполне нормальные пропорции самого тела, а костный возраст детей соответствует их календарному возрасту.
При наличии тиреотоксикоза резкое ускорение роста может сочетаться с похудением и многими другими симптомами. Также высокий рост будет характерным и для особого генетического синдрома, наследственно обусловленного – синдром Марфана. Этот синдром сочетается с резким удлинением конечностей, формированием узой грудной клетки и длинными пальцами на руках и ногах (паучьи пальцы). При наличии преждевременного полового созревания наличие высокого роста может сочетаться с ускорением костного возраста ребенка. При лечении проявлений гигантизма врач-эндокринолог будет назначать ребенку антагонисты гормона роста. Это буду синтетические аналоги гормона – соматостатина, препараты бромкриптин или октреотид. Иногда родители могут обращаться с просьами замедления роста девочек, особенно если по прогнозам ее окончательный рост может превышать 180-185 см. с этими целями ей вводится специальный женский половой гормон – эстроген. Такой метод будет эффективным, если костный возраст девочек еще не достиг по значениям десяти лет. При этом окончательный рост можно уменьшить примерно на 10-15 см.
Значительно чаще будет отмечаться замедление роста, и оно вызывает гораздо большее беспокойство со стороны родителей ребенка. Обычно рост замедляется в результате влияния различных тяжелых нарушений в питании или при наличии хронических болезней. Такое состояние обычно никаких проблем не представляет, его легко можно распознать при обследовании. При целом ряже генетических патологий, которые могут сопровождаться нарушением в росте костей – это так называемые хондродистрофии, жалобы будут другими. Сам по себе замедленный рост костей обычно не будет основным поводом для беспокойства, но родителей будет сильно беспокоить изменение пропорций ребенка или изменение в форме костей. Таких больных ранее было принято называть карликами, и многие из таких детей в дальнейшем служили придворными шутами у королей и вельмож. До настоящего времени эти виды заболеваний практически не поддаются лечению.
От подобных состояний стоит также отличать вариант семейной низкорослости у детей, при которой, даже учитывая выраженное отставание в росте от всех своих сверстников, костный возраст ребенка будет соответствовать календарному. При этом темпы полового развития будут вполне нормальными, и такие подростки достигают роста, который определен по той формуле, что мы приводили выше. Естественно, что родителей просто не может не обеспокоить наличие конституциональной формы отставания ребенка по росту. При подобной форме проблемы родители могут замечать замедленные темпы роста ребенка, а часто и набора веса, соответственно росту. Обычно это происходит со второго года жизни малыша, когда его прибавки в росте не могут достигать даже половины от нормальных, и составляют примерно 3-5 см в год. Темпы роста остаются пониженными на протяжении последующих 1-3 лет, но затем происходит ускорение роста до привычных норм. У таких детей и сроки костного возраста, и начало периода полового созревания будут отставать также на примерно те же 1-3 года, то есть на те сроки, в которые происходило замедление роста. Однако, окончательные показатели роста в целом достигают своих генетических особенностей.
Низкорослость также может развиваться в результате выраженного дефицита в количестве гормона роста. Такие формы проблем роста носят название гипофизарного нанизма. Страдающих этим заболеванием людей часто и обидно называют лилипутами. Основные причины данного врожденного заболевания на сегодня не выяснены, и в редких случаях они могут быть связаны с повреждением гипофиза, развитием в нем опухолей. При врожденных формах будет заметно пропорциональное отставание в росте уже примерно к одному году, и далее, в последующем дети могут прибавлять в росте крайне незначительно. Помимо этого, нарушения в функциях гипофиза может одновременно приводить к недоразвитости половых органов. Об этом можно говорить у мальчиков при маленьких размерах полового члена (менее 2.8 см) уже в первые дни и месяцы жизни. Часто такие заболевания сочетаются со многими из других эндокринных нарушений, к примеру, со сниженным уровнем сахара в крови (гипогликемия) или с нарушениями дыхания и приступами синюшности.
Завтра продолжим.
Еще статьи на тему “Гипофиз”:
Что такое гипофиз и какие нарушения бывают?
Патологии гипофиза. Аденома гипофиза
Симптомы и лечение аденомы гипофиза
Источник
Рост – это один из наиболее важных показателей здоровья ребенка.
Эта статья посвящена гипопитуитаризму – заболеванию эндокринной системы с изолированным дефицитом гормона роста (соматотропный гормон) или множественным дефицитом гормонов, которые вырабатывает гипофиз.
Важно знать причины, особенно, генетические механизмы развития заболевания, а также классификацию этой патологии, клиническая картина и ее варианты, диагностика и критерии направления к детскому эндокринологу, и необходимые обследования в рамках наблюдения ребенка с гипопитуитаризмом.
Что такое гипофиз и почему возникает гипопитуитаризм
Гипопитуитаризм – эндокринная патология, которая характеризуется снижением или полным отсутствием секреции одного (соматотропный или гормон роста) или более гормонов гипофиза.
Гипофиз – это основная железа эндокринной системы, что входит в гипоталамо-гипофизарную систему, контролирующую функционирование периферийных эндокринных желез.
Этот термин от латинского слова hypophysis, что означает «отросток» и имеет следующие синонимические названия как «нижний придаток мозга» или «питуитарная железа».
Эта эндокринная железа расположена в центральной части головного мозга на турецком седле, хорошо защищена подкоркой правого и левого полушарий.
Какие гормоны продуцирует гипофиз
Гормоны выделяет передняя доля – аденогипофиз, задняя доля гипофиза выполняет нейроэндокринную функцию и участвует в стабилизации артериального давления и водно-солевого баланса. Промежуточная доля соединяет эти доли и является проводником сигналов от гипоталамуса.
Нарушения в строении или функционировании гипофиза вызывают патологические изменения в организме, связанные с недостатком продукции гормонов:
- соматотропный гормон (СТГ) – влияет на роста всех клеток организма, интеллектуальное и физиологическое развитие, обмен веществ;
- тиреотропный гормон (ТТГ) – активирует работу щитовидной железы и продукции ее гормонов, а также фосфолипидов и нуклеиновой кислоты;
- адренокортикотропный гормон (АКТГ) – активирует работу гормонов коры надпочечников (кортизола, кортизона и кортикостерона);
- гонадотропные гормоны (лютеинизирующий и фолликулостимулирующий гормон ЛГ и ФСГ) – стимуляторы секреции гормонов половыми железами;
- пролактин – гормон стимулирующий рост молочных желез, лактацию, регулирующий функцию половых желез (яичников или яичек) и иммунные процессы.
Гипопитуитаризм связан с недостатком продукции соматотропного гормона (изолированная соматотропная недостаточность) и других гормонов гипофиза (пангипопитуитаризм).
Возможно более позднее развитие дефицита других гормонов гипофиза через несколько лет после манифестации изолированной соматотропной недостаточности.
В связи с этим развиваются симптомы, которые характеризуют недостаток действия этих гормонов в организме – гипотиреоз, гипокортицизм, гипогонадизм (задержка или отсутствие полового созревания), несахарный диабет.
Причины
Выделяют врожденный гипопитуитаризм и приобретенный гипопитуитаризм.
Врожденный гипопитуитаризм может развиваться в результате:
- пренатальной и родовой травмы;
- внутриутробного поражения структур гипофиза – дефекты развития (гипоплазии или аплазии);
- мутациями в генах, контролирующих продукцию СТГ.
Помимо этого, врожденный гипопитуитаризм может являться составной частью врожденных «синдромов дефекта среднего мозга». Наиболее частой патологией в этой группе является септооптическая дисплазия, характеризующаяся агенезией/гипоплазией зрительных нервов, прозрачной перегородки и мозолистого тела, и разной степенью нарушения зрения.
Приобретенный гипопитуитаризм возникает:
- после травм головы;
- после хирургических вмешательств в связи с повреждением гипофизарной ножки;
- появления опухолей гипофизарно-гипоталамической области;
- при облучении головы и шеи (при лейкозе, лимфогранулематозе, ретинобластоме);
- после проведения химиотерапии;
- воспаления (энцефалит и менингит, аутоиммунный гипофизит);
- сосудистых патологий – аневризмы сосудов гипофиза, инфаркт гипофиза.
Наследственные формы гипопитуитаризма
Генетическая основа дефицита гормона роста при наличии родственников первой степени родства с той же патологией (с ростом ≤3 стандартных отклонений (SDS)).Они встречаются в 5—30% случаев.
Выделяют наследственный изолированный дефицит гормона роста (ИДГР) или множественный дефект гормонов аденогипофиза (МДГА)
Наследственный изолированный дефицит СТГ ассоциирован с 5 типами различных заболеваний:
- Тип 1А и 1В, которые наследуются по аутосомно-рецессивному типу – у каждого из родителей должен присутствовать соответствующий дефектный ген GH – I (грубые мутации или делеции).
- Тип II наследуется по аутосомно-доминантному типу – один из родителей болен ИДГР.
- Тип III – наследуется как сцепленный с Х – хромосомой и сочетается с гипоглобулинемиями.
Тип 1А протекает значительно тяжелее – отмечается выраженная задержка роста и тяжелый дефицит соматотропного гормона, у детей всегда возникают гипогликемические состояния.
При всех этих формах отмечаются низкие уровни продукции СТГ после проведения проб, для уточнения диагноза проводится молекулярно-генетическое обследование.
Заболевания, с множественным дефицитом гормонов аденогипофиза связаны с мутациями в генах, кодирующих гипофизарные транскрипционные факторы, участвующие в эмбриогенезе аденогипофиза. К данным генам относятся гены: POU1F1 (PIT-1), PROP-1, LHX-3, LHX-4, HESX-1, Pitx2
Большинство мутаций гена PIT-1, который регулирует развитие гипофиза в периоде эмбрионального развития, обнаруженных на сегодняшний день, имеют рецессивный характер наследования (т.е должны присутствовать у обеих родителей важный фактор – близкородственные браки. При этой генной мутации отмечается дефицит гормона роста и пролактина, с возможным снижением секреции гормонов щитовидной железы.
Ген PROP1 (prophet of Pit1) кодирует одноименный белок, который так же, как и PIT-1, является фактором транскрипции. Дефект данного гена является наиболее часто встречающейся генетической причиной при гипопитуитаризме (соматотропной недостаточности), к которой часто в течение жизни присоединяются гипогонадизм (нарушения полового созревания, чаще в подростковом возрасте) и гипокортицизм у подростков или даже после 20-30 лет жизни. Поэтому детей необходимо наблюдать длительно. Важно помнить, что в 20 % случаев при данной генетической патологии отмечается гиперплазия (увеличение) гипофиза при обследовании МРТ, которая проходит самостоятельно и не требует оперативного вмешательства. В настоящее время подобная МРТ-картина у ребенка любого возраста с дефицитом СТГ/Пролактина/ТТГ является показанием для молекулярной диагностики, в первую очередь, для анализа гена PROP-1.
Особенности приобретенных форм болезни
Особенностью приобретенной соматотропной недостаточности, вне зависимости от причин ее возникновения, является тот факт, что она в большинстве случаев сочетается с дефицитом других тропных гормонов (ТТГ, АКТГ, ЛГ и ФСГ), однако «выпадение» гипофизарных гормонов происходит не одновременно, а имеет определенную стадийность.
Вместе с тем секреция соматотропного гормона, являясь, по-видимому, наиболее чувствительной к действию повреждающего фактора, страдает в первую очередь. Гораздо реже развивается несахарный диабет (при поражении гипоталамических ядер или повреждении воронки гипофиза).
Главные причины:
- Опухоли гипоталамуса и гипофиза
(краниофарингиома, аденома гипофиза). - Опухоли других отделов мозга
(глиома зрительного нерва). - Травмы (черепно-мозговая травма, хирургическое повреждение ножки гипофиза).
- Инфекции (вирусный или бактериальный энцефалит и менингит, неспецифический гипофизит).
- Супраселлярные арахноидальные кисты, гидроцефалия, синдром «пустого турецкого седла»
- Сосудистая патология (аневризмы сосудов гипофиза, инфаркт гипофиза).
- Облучение головы и области шеи (лейкемия, ретинобластома, другие опухоли головы и шеи, общее облучение всего тела (например, пересадка костного мозга).
- Токсическое воздействие химиотерапии.
- Инфильтративные болезни (гистиоцитоз, саркоидоз).
врач-педиатр, детский эндокринолог Сазонова Ольга Ивановна
Источник
