Гормоны повышены у ребенка 4 года
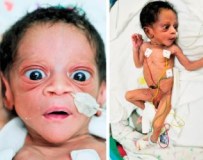
Гипертиреоз у детей – это клинический синдром, который характеризуется повышенной выработкой тиреоидных гормонов. Возникает при диффузном токсическом зобе, аденоме гипофиза, на начальных стадиях тиреоидитов. Основные симптомы: ускорение обмена веществ, психоэмоциональные нарушения, дисфункция пищеварительной и сердечно-сосудистой системы. Диагностика синдрома предполагает УЗИ и сцинтиграфию щитовидной железы, развернутый анализ тиреоидного гормонального профиля и специфических антител. Лечение состоит из тиреостатической терапии, препаратов радиоактивного йода и бета-адреноблокаторов.
Общие сведения
Гипертиреоз встречается с частотой до 20-25 больных на 100 тыс. детского населения. В основном болеют дети предпубертатного и пубертатного возраста, причем девочки в 6-8 раз чаще мальчиков. У младенцев и детей раннего возраста симптомы гипертиреоза определяются не чаще 8 случаев на 1 млн населения. Термины гипертиреоз и тиреотоксикоз обычно используются как синонимы, хотя первый обозначает гиперфункцию щитовидной железы (ЩЖ), а второй – токсические эффекты тиреоидных гормонов на ткани. Зачастую у ребенка развиваются оба состояния, но иногда гипертиреоз может быть изолированным.

Гипертиреоз у детей
Причины
У новорожденных гиперфункция ЩЖ зачастую связана с наличием токсического зоба у матери. При этом в организме беременной вырабатываются специфические антитела, которые проникают через плаценту к плоду, присоединяются к рецепторам тироцитов и усиливают синтез гормонов. У старших детей гипертиреоз провоцируется следующими причинами:
- Болезнь Грейвса. Диффузный токсический зоб составляет до 90% причин патологии в детском возрасте. Вследствие постоянной стимуляции ТТГ-рецепторов тироцитов щитовидная железа равномерно увеличивается, а ее гормональная функция усиливается. Изредка гипертиреоз формируется при многоузловом токсическом зобе.
- Тиреоидит Хашимото. Усиление синтеза и выделения тиреоидных гормонов наблюдается в гипертиреоидной фазе, которая чаще возникает у детей в начале заболевания. Аутоиммунные процессы стимулируют щитовидную железу и частично разрушают клетки, усиливая выход гормональных биомолекул в кровоток.
- Другие виды тиреоидитов. Иногда симптомы тиреоидной гиперфункции выявляются у детей с острым тиреоидитом, вызванным бактериальной флорой. Тиреоидная гиперфункция также возможна при подостром тиреоидном воспалении, которое спровоцировано вирусными агентами.
- Аденома гипофиза. При гормонально активной опухоли центрального эндокринного органа усиливается синтез ТТГ, который стимулирует тироциты и увеличивает продукцию тироксина и трийодтиронина. Подобные нарушения бывают и при патологии гипоталамуса, секретирующего тиролиберины.
Патогенез
Усиление выработки тиреоидных гормонов в щитовидной железе вызвано либо тиреостимулирующими антителами, либо повышением концентрации гормональных регуляторов (ТТГ и тиролиберинов) в крови. В результате этих механизмов в системный кровоток поступает неадекватное количество Т3 и Т4, которые связываются с клеточными рецепторами в разных тканях и оказывают негативные физиологические эффекты.
В норме тиреоидные гормоны участвуют во многих биохимических процессах, поэтому их избыток сопровождается системными нарушениями. У детей возникают патологические катаболические процессы, нарушается углеводный и липидный обмен. Гормоны оказывают токсическое влияние на сердечно-сосудистую и нервную систему, в период детства негативно воздействуют на психику.
Классификация
В зависимости от локализации патологии выделяют 3 типа гипертиреоза: первичный, который обусловлен поражением на уровне щитовидной железы, вторичный, характеризующийся нарушениями работы гипофиза, и третичный, связанный с заболеваниями гипоталамуса. В практической детской эндокринологии важна классификация синдрома по клиническим проявлениям, в которой различают 3 варианта:
- Субклинический. Представляет собой легкую степень тяжести гипертиреоза. Клинические симптомы отсутствуют или минимально выражены. Диагноз устанавливается только на основании изменений гормонального профиля.
- Манифестный. Классическое течение гипертиреоза, которое относится к среднетяжелой степени, характеризуется развернутой клинической картиной в сочетании с лабораторными изменениями.
- Осложненный. Неблагоприятный вариант течения, когда типичные симптомы гипертиреоза дополняются признаками поражения сердца, нервной системы и паренхиматозных органов.
Симптомы гипертиреоза у детей
У младенцев клинические проявления возникают в первый месяц жизни. Они включают кишечные расстройства (рвоту, диарею), проблемы с грудным вскармливанием, повышенное беспокойство и нарушения сна. Иногда у новорожденного видна увеличенная щитовидная железа. Зачастую при неонатальном гипертиреозе отмечается регресс симптоматики в течение первого полугодия жизни.
По завершении периода новорожденности среди ведущих признаков гипертиреоза преобладают психоэмоциональные симптомы. У детей появляется беспричинная раздражительность, гиперактивность, капризность и склонность к агрессии. Школьники хуже успевают в учебе, поскольку им становится сложно прилагать волевые усилия и длительно концентрироваться на одном деле.
Физиологические симптомы представлены непереносимостью жары и духоты, усиленным потоотделением, дрожанием пальцев рук. Многие дети жалуются на неприятное чувство сердцебиения, головные боли, которые вызваны повышением артериального давления. Кишечные признаки включают учащение дефекации, периодически спазмы в кишечнике. Ребенок стремительно худеет, хотя аппетит у него не нарушен.
Еще одна группа клинических проявлений включает симптомы основной патологии, которая спровоцировала тиреоидную гиперфункцию. При остром тиреоидите – фебрильная лихорадка, сильные боли по передней поверхности шеи, нарушения глотания, при подострой форме – субфебрильная температура, умеренная болезненность в проекции органа. Выпячивание глаз (экзофтальм) встречается только при гипертиреозе, вызванном болезнью Грейвса.
Осложнения
У детей, страдающих неонатальным гипертиреозом с тиреотоксикозом, риск негативных последствий варьирует в пределах 10-15%. У младенцев возникают нарушения психомоторного развития, задержка роста, а также краниосиностоз – слишком раннее окостенении черепных швов, из-за чего формируется микрокрания. Несовременно диагностированный гипертиреоз у новорожденного может иметь летальный исход.
Во всех возрастных группах самым тяжелым осложнением заболевания является тиреотоксический криз, который без экстренной медицинской помощи может закончиться смертью ребенка. Неотложное состояние проявляется жизнеугрожающими аритмиями, гипертензивным кризом, острой сердечной недостаточностью. Затем начинается делирий, который переходит в кому и смерть.
Диагностика
При физикальном осмотре детский эндокринолог обращает внимание на увеличение щитовидной железы, появление функциональных шумов сердца при аускультации, наличие патологических глазных симптомов. При оценке неврологического статуса врач, как правило, выявляет снижение мышечной силы и тонуса. Затем проводится инструментальная и лабораторная диагностика гипертиреоза:
- УЗИ щитовидной железы. При аутоиммунном тиреоидите и диффузном зобе визуализируют увеличенную железу с неоднородной структурой. Для многоузлового зоба характерны отдельные патологические очаги на фоне нормальной паренхимы органа. Неблагоприятным признаком считается гипоэхогенное образование с нечеткими контурами и кальцификатами.
- Сцинтиграфия щитовидной железы. Исследование выполняется для детальной оценки функциональной активности органа. При гипертиреозе наблюдается повышенный захват радиофармпрепарата, изредка на результатах сцинтиграфии видны отдельные «горячие узлы».
- ЭКГ. Данные электрокардиографии необходимы, чтобы оценить, как функционирует сердечно-сосудистая система и выявить ее вторичное поражение. Если эндокринолог видит патологические признаки на ЭКГ, он дополнительно назначает ЭхоКГ, консультацию детского кардиолога.
- Гормональные исследования. При гипертиреозе в крови повышены уровни свободного Т3, Т4, увеличен титр антител к тиреопероксидазе (ТПО), тиреоглобулину (ТГ), рецепторам ТТГ. Уровень гипофизарного гормона ТТГ снижен при первичной форме расстройства, повышен при вторичном и третичном гипертиреозе.
Лечение гипертиреоза у детей
Консервативная терапия
При тиреотоксикозе ограничивают физическую активность, чтобы не усугублять нарушения терморегуляции и не создавать чрезмерную нагрузку на сердечную мышцу. Детям запрещено давать кофе и крепкий чай, подросткам категорически нельзя употреблять энергетики и спиртные напитки. До нормализации гормонального фона ограничивают поступление в организм йода с контрастными веществами. Медикаментозное лечение гипертиреоза включает:
- Тиреостатики. Препараты используются для подавления гормональной продукции и нормализации состояния здоровья ребенка. Терапия проводится 1-1,5 года. Лечение предполагает постоянный контроль уровня свободного Т4 и постепенное введение заместительного лечения левотироксином.
- Радиоактивный йод. Такая схема используется после длительного и безуспешного применения терапии тиреостатиками. Назначение йода возможно у детей старше 5 лет с выраженным гипертиреозом и тиреотоксикозом.
- Бета-адреноблокаторы. Лекарства нормализуют частоту сердечных сокращений и повышают эффективность работы миокарда. Они устраняют симптомы, предупреждают развитие тяжелых кардиальных осложнений гипертиреоза.
Хирургическое лечение
Оперативное вмешательство (тиреоидэктомия) выполняется детям с рецидивирующим гипертиреозом, при неэффективности медикаментозной терапии на протяжении 12-18 месяцев, наличии крупных узловых новообразований. Перед хирургическим лечением ребенку рекомендована терапия тиреостатиками до достижения состояния эутиреоза. После операции проводят контроль паратгормона и кальция, по показаниям назначают витамин D.
Прогноз и профилактика
При своевременном начале лечения стойкая ремиссия наступает у 75% детей. Прогноз зависит от причины и степени повышения уровня тиреоидных гормонов, скорости уменьшения зоба и наличия у пациента сопутствующих заболеваний. Первичная профилактика гипертиреоза заключается в предупреждении эндокринных болезней, сопровождающихся нарушением функции щитовидной железы.
Источник
Часть 1
Гиперпролактинемия (ГП) – симптомокомплекс, возникающий на фоне повышенного содержания пролактина (П) в крови. ГП проявляется прежде всего угнетающим влиянием на репродуктивную функцию и нормальный процесс полового развития. Подавляющее число работ посвящено исследованиям ГП у женщин. В популяции детей и подростков гиперпролактинемию выявляют у 5%. Имеются лишь отрывочные сведения о влиянии избытка П на их организм. Скудные и неспецифические проявления этого синдрома, отсутствие типичной симптоматики у детей и подростков лежат в основе запоздалой диагностики [1].
Физиология пролактина
Пролактин (лактотропный гормон, маммотропин, лютеотропин) синтезируется лактотрофами передней доли гипофиза, составляющими около 20% его массы. Специфический для гипофиза транскрипционный фактор (Pit-1) присутствует в ядрах лактотрофов, соматотрофов, тиреотрофов. Он стимулирует экспрессию гена пролактина, соматотропина, тиреотропина. Некоторые клетки гипофиза, выделяющие П, способны синтезировать и соматотропный гормон гипофиза (СТГ). Помимо гипофиза, П секретируют клетки центральной нервной системы, тимоциты, лимфоциты, эпителий молочных желез. Рецепторы к П идентифицированы во всех тканях организма. Ген пролактолиберина и его рецептора выявляется как в клетках нормального гипофиза, так и в секретирующих опухолях гипофиза.
Существует несколько изоформ П – мономерная, димерная и полимерная. Мономерная форма обладает максимальной активностью. Молекулярная масса его составляет 22,5 кДа. Большой пролактин (Big-пролактин) имеет молекулярную массу 50-60 кДа, является димером или тримером П, характеризуется более низкой аффинностью к рецепторам. Очень большой П (Big-big-пролактин), или макропролактин, имеет молекулярную массу 100-150 кДа. В связи с большим размером его молекул он не способен проникать через мембрану капилляров, поэтому не имеет биологической активности и медленно выводится почками. Разнообразием изоформ П можно объяснить в некоторых случаях отсутствие клинических симптомов при ГП [2].
Основным регулятором секреции пролактина является дофамин, который синтезируется в паравентрикулярных, серобугорных и дугообразных ядрах гипоталамуса. По воротной системе сосудов этот биогенный пептид попадает в гипофиз. П единственный из гормонов передней доли гипофиза, который находится под тоническим ингибирующим влиянием гипоталамуса. Дофамин и его агонисты стимулируют D2-рецепторы, что приводит к ингибированию высвобождения и секреции П. В свою очередь П по принципу обратной связи блокирует выработку дофамина.
В период вскармливания высокий уровень П поддерживается раздражением сосков, за счет рефлекторного усиления серотонинергического воздействия.
Количество пролактина увеличивается при стрессе, травмах. Стимулируют выработку этого гормона психотропные средства, алкоголь, наркотики.
Прогестерон снижает секрецию П в гипофизе, воздействуя непосредственно на него и, возможно, через гипоталамус. Ингибиторами выработки П также являются соматостатин и гамма-аминомасляная кислота.
Секреция П гипофизом обнаруживается уже в эмбриональном периоде. У плода концентрация его постепенно увеличивается. После рождения происходит снижение уровня П в течение 1-1,5 месяцев. Стимулирующее влияние на секрецию П оказывают эстрогены, тиролиберин (ТРГ). До пубертатного периода содержание П в крови девочек и мальчиков примерно одинаково. В подростковом возрасте у девушек уровень П возрастает, а у большинства юношей не изменяется.
Секреция П гипофизом в течение суток подчинена циклическим колебаниям, что связано с циркадными биологическими ритмами. Максимальная секреция П фиксируется через 1-1,5 часа после засыпания и снижается в дневное время. Период полураспада П составляет 20-30 минут.
Основное биологическое действие П – это влияние на репродукцию.
В женском организме П влияет на менструальный цикл. Избыток П тормозит овуляционный цикл, ингибируя фолликулостимулирующий гормон (ФСГ) и гонадотропин-релизинг-гормон (ЛГ-РГ). Он способствует пролонгированию желтого тела в яичниках (лютеиновая фаза цикла), тормозит овуляцию (при наступлении новой беременности), снижает секрецию эстрогенов и прогестерона. Обеспечивает контрацептивный эффект у кормящей женщины [3].
В период полового созревания влияет на рост грудных желез, увеличивая число секреторных долек и развитие сети протоков. Во время беременности П подготавливает молочные железы к лактации. После рождения ребенка, когда уровень эстрогенов у женщины падает, высокий уровень П у кормящей матери поддерживают механорецепторы соска. Сосательный рефлекс одновременно способствует образованию окситоцина в задней доле гипофиза и выделению молока.
В мужском организме П потенцирует действие лютеинизирующего гормона (ЛГ) и ФСГ, стимулируя клетки Лейдига. Влияет на объем тестикул и семенных пузырьков, за счет потенцирования активности тканевого фермента 5а-редуктазы, которая превращает тестостерон в 5а-дигидротестостерон (ДГТ), обладающий максимальной андрогеновой активностью. Регулирует активность сперматозоидов, усиливает их движение к яйцеклетке. П стимулирует выработку в надпочечниках дегидроэпиандростерон (ДГЭА) и дегидроэпиандростерон-сульфат (ДГЭА-С) [1].
Причины гиперпролактинемии
Выделяют физиологическую, биохимическую и патологическую гиперпролактинемию [4].
Физиологическая ГП
В норме уровень П достигает максимальных значений во время стадии «быстрого» сна или рано утром, в течение беременности.
Кормление грудью, а также стресс сопровождается резким увеличением содержания П в крови.
В периоде новорожденности у детей обоего пола уровень П высокий и клинически проявляется увеличением грудных желез. У девочек этот симптом обозначается как физиологическое телархе, а у мальчиков – как физиологическая гинекомастия. Механизм увеличения в той или иной степени грудных желез в периоде новорожденности связывают с подъемом уровня гипофизарных гормонов ФСГ и ЛГ, пролактина. К концу месяца концентрация половых гормонов и П у них сопоставима с уровнем взрослых людей. К 3-4 месяцам жизни происходит снижение. Другие считают, что нагрубание грудных желез обусловлено эффектом материнских эстрогенов и пролактина, которые ребенок получает с грудным молоком.
У юношей в 50% случаев при сопутствующей физиологической гинекомастии отмечается транзиторное повышение уровня П.
Биохимическая ГП
Причиной биохимической ГП является феномен макропролактинемии, при котором значительная часть П в сыворотке крови представлена big-big-пролактином (макропролактин). Частота данного феномена по разным данным от 15% до 35% среди всех случаев ГП, а при уровне П от 1000 до 2000 мЕд/л достигает 50%.
Массовое определение уровня макропролактина в клинической практике стало возможным благодаря появлению дешевого и удобного метода полиэтиленгликоль-преципитации (ПЭГ). Определение П обычными методами в интактной и осажденной сыворотках позволяет вычислить соотношения макропролактина и мономерного пролактина. В норме макропролактин составляет 9-21% от общего количества П.
Макропролактинемией считается доля макропролактина больше 60%. При содержании макропролактина менее 40% макропролактинемию можно исключить. Если доля макропролактина составляет от 40% до 60%, то результаты анализа следует считать недостоверными, требуется его повторное проведение.
Высокомолекулярный П может связываться с антителами и плохо выделяться из организма. Макропролактинемия протекает бессимптомно или сопровождается стертой симптоматикой и, как правило, лечения не требует. Исключением является ситуации, когда при преобладании макропролактина абсолютная концентрация мономерного пролактина также повышена. Таким образом, макропролактинемия является в большей степени лабораторным феноменом, чем клиническим [5].
Патологическая ГП
В патологической гиперпролактинемии выделяют гиперпролактинемический гипогонадизм, связанный с наличием пролактина, и идиопатический; гиперпролактинемию в сочетании с другими гипоталамо-гипофизарными заболеваниями; симптоматическую ГП [4].
Гиперпролактинемический гипогонадизм связан с нарушением гипоталамической регуляции П (тонического дофаминергического ингибирующего влияния) вследствие снижения образования пролактостатина (дофамина) или усиления продукции пролактолиберина, что приводит к гиперплазии лактотрофов с возможным развитием микро- или макроаденомы.
Длительно существующая ГП подавляет секрецию гонадотропных гормонов (ФСГ и ЛГ) и блокирует процесс стероидогенеза в гонадах, способствуя формированию синдрома гипогонадизма, который является составной частью синдрома ГП.
Пролактин-секретирующие аденомы являются самыми частыми опухолями гипофиза. Различают микроаденомы (размером менее 1 см), макроаденомы (более 1 см) и гигантские (более 4 см). Макроаденомы встречаются редко (около 10% пролактином), в основном у лиц мужского пола (соотношение микро- и макроаденом – 10:1 у женщин и 1:1 у мужчин).
Это, по-видимому, связано с меньшей выраженностью симптомов и более поздним выявлением. Возраст больных варьирует от 2 до 80 лет, чаще болеют женщины репродуктивного возраста.
У детей пролактиномы встречаются редко, более характерны макропролактиномы [6, 7]. По характеру роста выделяют инвазивные и неинвазивные пролактиномы, в зависимости от наличия или отсутствия прорастания в кавернозный синус.
Идиопатическая ГП
По некоторым данным наиболее часто встречается идиопатическая ГП, однако этиология и патогенез ее до конца не ясен. Предполагается, что гиперпролактинемия, микроаденомы и макроаденомы являются стадиями одного процесса, запускающегося в результате снижения влияния дофамина.
Другие авторы считают, что пролактиномы это следствие соматической мутации и к идиопатической гиперпролактинемии отношения не имеют. Возможно, развитие идиопатической или функциональной лактотропной дисфункции программируется на ранних этапах внутриутробного развития вследствие гипоксии гипоталамуса, что может вызывать нейротрансмиттерные нарушения, приводящие к дефектам дофаминергичекого контроля. Описаны семейные случаи, что говорит о роли наследственной патологии в генезе данного заболевания [8].
При наличии макроаденомы гипофиза первыми жалобами могут являться головные боли, головокружения, сужение полей зрения, увеличение массы тела, задержка полового развития, а у мальчиков увеличение грудных желез.
Гиперпролактинемия в сочетании с несекретирующимии опухолями гипоталамо-гипофизарной области, которые влияют на транспорт дофамина, вторично могут повышать концентрацию П. Подобное наблюдается при сдавлении ножки гипофиза гормоннепродуцирующими опухолями, а также опухолями гипофиза, которые кроме пролактина продуцируют соматотропный, адренокортикотропный гормоны, и другими объемными образованиями – краниофарингиомами, глиомами, менингиомами, эктопическими пинеаломами.
При синдроме пустого турецкого седла гипофизарный контроль ослабевает из-за изменения анатомии хиазмально-селлярной области. Регуляцию секреции пролактина нарушают инфильтративные процессы гипоталамо-гипофизарной области при системных заболеваниях (гистиоцитоз, саркоидоз, сифилис, туберкулез), лимфоцитарном гипофизите, сосудистых нарушениях, механическом и лучевом повреждениях гипоталамо-гипофизарной области [4].
Пролактинома чаще встречается у девочек пубертатного периода и проявляется задержкой физического и полового развития. В некоторых случаях единственным симптомом ГП у них является нарушение менструального цикла. У девочек наблюдается позднее менархе, первичная аменорея и галакторея. Впоследствии обнаруживается гипоплазия наружных половых органов и молочных желез.
При развитии гиперпролактинемии в позднем возрасте возможны различные нарушения менструальной функции: нерегулярные менструации, олиго-, опсо-, альго-, вторичная аменорея, реже обильные маточные кровотечения или ановуляторный цикл. Может снижаться либидо, появляется сухость влагалища, гипоплазия матки вследствие гипоэстрогении.
Появление или усиление гирсутизма, особенно у больных с олигоаменореей и аменореей, может быть обусловлено ГП. Повышение секреции П напрямую стимулирует стероидогенез в надпочечниках, поэтому у больных с аденомой гипофиза существенно увеличивается содержание ДГЭА и ДГЭА-С при умеренной тестостеронемии.
Галакторея, не связанная с беременностью или кормлением, варьирует от выделения нескольких капель при надавливании на железу до самопроизвольного истечения. Выраженность этого симптома зависит от уровня эстрогенов. В старшем возрасте ГП ведет к снижению полового влечения и потенции, а также к бесплодию. Недостаточность эстрогенов при ГП служит причиной повышения массы тела, задержки жидкости, остеопороза.
У мальчиков в препубертатном периоде развиваются евнухоидные пропорции тела: относительно длинные конечности, высокая талия, бедра относительно шире пояса нижних конечностей, отложение жира в области сосков, живота, у гребешков подвздошных костей, мышцы дряблые, слабые, голос высокий детский. Тестикулы умеренно гипоплазированы. В пубертатном периоде могут отсутствовать вторичные половые признаки, половое влечение, фертильность. У подростков галакторея встречается редко, т. к. они предварительно не эстрогенизированы.
Конституциональная задержка полового развития (КЗПР)
Одной из предполагаемых причин задержки полового созревания у таких подростков является функциональная гиперпролактинемия. Факт повышения уровня П в ответ на стимуляционные пробы с хлорпропамидом и ТРГ, а также повышение суточного пула П отмечают у детей с КЗПР. Эти пробы отличают задержку пубертата от гипогонадотропного гипогонадизма, при котором уровень П снижен.
Функционально ГП может быть связана с ослаблением дофаминергического тонуса, что приводит к снижению импульсной секреции как гонадотропных гормонов, так и гормонов роста. В физиологических условиях П тормозит образование 5α-дигидротестостерона из тестостерона за счет снижения активности 5α-редуктазы. Кроме того, ГП может оказывать непосредственное ингибирующее влияние на секрецию гонадотропных гормонов [9].
ГП на фоне гипотиреоза развивается в ответ на снижение уровня тиреоидных гормонов и повышения секреции ТРГ. Тиреолиберин является одним из основных факторов, стимулирующих как секрецию П, так и тиреотропного гормона гипофиза (ТТГ). Повышение его концентрации приводит к гиперсекреции этих двух гормонов.
Возможно, что ТРГ оказывает стимулирующее влияние на секрецию П через повышение экспрессии генов пролактолиберина и рецепторов к нему непосредственно в гипофизе. При длительном некомпенсируемом первичном гипотиреозе нередко выявляется гиперплазия гипофиза [9]. Подтверждением может служить редко встречающийся синдром Ван-Вика Громбаха у мальчиков, который характеризуется тяжелым декомпенсированным гипотиреозом, преждевременным половым развитием, гинекомастией, увеличением тестикул. У этих больных выявляется значительное повышение уровеней ТТГ, П и гонадотропных гормонов. Низкую концентрацию тестостерона некоторые авторы объясняют ингибирующим действием П.
Адекватная заместительная терапия гипотиреоза тиреоидными гормонами нормализует секрецию П и ликвидирует гинекомастию.
Гинекомастия
Гинекомастия – увеличение грудных желез у мальчиков, может быть одним из симптомов гиперпролактинемии. В пубертатном периоде физиологическая гинекомастия встречается у большинства подростков. Увеличение железистой ткани, как правило, симметричное, ареолы уплотнены, могут быть болезненны и совпадают с 3-4 стадией полового развития. Основным органом-мишенью П являются молочные железы. Этот гормон стимулирует рост и развитие молочных желез и увеличивает число долек и протоков в них.
Предполагают, что одной из причин гинекомастии является избыточная конверсия эстрогенов из андрогенов в результате повышенной ароматазной активности. У некоторых юношей увеличение молочных желез визуально неотличимо от железистой ткани девушек-подростков. В большинстве случаев физиологическая гинекомастия не требует лечения и самостоятельно проходит через 1-2 года. У части юношей гинекомастия сохраняется после завершения пубертата, тогда ее относят к персистирующей гинекомастии. Галакторея у подростков встречается редко, так как они предварительно не эстрогенизированы.
Лечение идиопатической гинекомастии не разработано. У некоторых больных уменьшается ткань молочных желез при применении тамоксифена (антиэстроген) и тестолактона (блокирует ароматазную активность).
Окончание статьи читайте в следующем номере.
В. В. Смирнов1, доктор медицинских наук, профессор
А. И. Морозкина
М. Д. Утев
ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
1 Контактная информация: smirnov-web@mail.ru
Источник
