Цитофлавин ребенку 4 года
Статьи
Опубликовано в журнале:
Журнал неврологии и психиатрии, 10, 2016
doi: 10.17116/jnevro201611610134-37
С.Ю. Лаврик1*, В.В. Шпрах2, С.В. Домитрак1, А.С. Борисов1
1 Клиника ГБОУ ВПО «Иркутский государственный медицинский университет», Иркутск, Россия; 2 ГБОУ ДПО «Иркутская государственная медицинская академия последипломного образования», Иркутск, Россия
Цель исследования. Изучение эффективности и безопасности комплексного метаболического нейропротектора цитофлавина у детей с последствиями перинатального гипоксического поражения ЦНС. Материал и методы. Монотерапия цитофлавином проводилась в течение 25 дней по 1 таблетке 2 раза в день в трех группах пациентов в возрасте 4-8 лет: с детским церебральным параличом – 35 детей, минимальной мозговой дисфункцией – 64 и сенсоневральной тугоухостью – 47. Контрольную группу составили 30 детей. До назначения цитофлавина и после завершения курса лечения проводили исследование неврологического статуса, нейрофизиологическое обследование и нейропсихофизиологическое тестирование. Результаты и заключение. Установлена эффективность цитофлавина у детей дошкольного и раннего школьного возраста, отмечено комплексное нейропротективное действие препарата, включающее вазоактивный, ноотропный и противоастенический эффекты. Побочных реакций на фоне приема препарата не наблюдалось.
Ключевые слова: детский церебральный паралич, сенсоневральная тугоухость, минимальная мозговая дисфункция, нейропсихофизиологическое тестирование, цитофлавин.
Cytoflavin in the treatment of preschool and early school age children with the consequences of perinatal hypoxic brain damages
S.Yu. Lavrick, V.V. Shprakh, S.V. Domitrak, A.S. Borisov
Clinic of Nervous Diseases of Irkutsk e Medical University, Irkutsk, Russia; Irkutsk e Medical Academy of Continuing Education, Irkutsk, Russia
Objective. To study the efficacy and safety of the complex bolic neuroprotector cytoflavin in children with the consequences of perinatal hypoxic brain damages. Material and methods. Patients, aged 4-8 years, were stratified into three groups: 35 with infant cerebral palsy, 64 with the minimal brain dys and 47 with sensorineural hearing loss. The control group consisted of 30 children. Monotherapy with cytoflavin was carried out in the dose of one tablet twice a day for 25 days. Neurologic us, neurophysiological examination andneuropsychophysiological testing were performed before and after treatment. Results and conclusion. The efficacy of cytoflavin in children of preschool and early school agewas demonstrated. A complex neuroprotective action, including vasoactive, nootropic and antiasthenic effects, was revealed. Side-effects of cytoflavin were not observed.
Keywords: infant cerebral palsy, sensorineural hearing loss, minimal cerebral dys, neuropsychophysiological testing, cytoflavin.
Перинатальные поражения ЦНС, обусловленные различными факторами риска и их сочетанием, составляют большую гетерогенную группу патологических состояний. Наиболее высок процент таких нарушений среди глубоко недоношенных новорожденных, родившихся в условиях острой и хронической гипоксии, что оказывает крайне неблагоприятное воздействие на развивающийся мозг, имеющий высокую потребность в энергии и глюкозе. Большинство исследователей считают, что после запуска нейротоксического каскада, связанного с гипоксически-ишемическим воздействием, процесс повреждения мозговой ткани может сохраняться длительное время, носить самоподдерживающийся характер за счет патологической возбудимости нейронов и феномена эксайтотоксичности, в связи с чем последствия перинатального поражения (ППП) ЦНС нередко отмечаются и в более отдаленных периодах жизни детей [1-7].
К неблагоприятным вариантам ППП ЦНС большинство авторов [4-7] относят детский церебральный паралич (ДЦП), сенсоневральную тугоухость (СНТ) и минимальную мозговую дисфункцию (ММД). На современном этапе термин ДЦП включает в себя большую группу резидуальных состояний с непрогрессирующим течением, частота которых обусловлена повреждением головного мозга на ранних этапах его развития [1, 2, 6, 7]. С учетом улучшения сурдологической помощи детям, СНТ также представляет собой весьма значимую медико-экономическую проблему: на 1000 новорожденных с нормальным слухом приходится 1 ребенок с выраженной степенью тугоухости, а нарушения слуха средней и легкой степени отмечаются у 1-2% новорожденных [8]. ММД характеризуется нарушением развития отдельных высших психических функций (ВПФ) при отсутствии выраженного снижения интеллекта, в сочетании с расстройствами поведения и эмоциональной сферы, приводящими в случае прогрессирования к социальной дезадаптации ребенка [3, 9-11]. По результатам собственных исследований, частота ММД у детей дошкольного и раннего школьного возраста в среднем составляет 11,9%.
Углубленная нейрофизиологическая и нейропсихофизиологическая диагностика позволяет выработать дифференцированные подходы к лечению и реабилитации детей с ППП ЦНС, являясь одним из перспективных направлений в неврологии детского возраста. Такие дети нуждаются в объективной оценке степени тяжести имеющихся клинических и нейропсихологических синдромов, последующем динамическом наблюдении и своевременном проведении комплекса лечебно-реабилитационных мероприятий, что позволяет оптимизировать темпы психомоторного развития, улучшая неврологический прогноз и социальную адаптацию [1, 2, 5, 6, 10].
Цель исследования – изучение клинико-нейрофизиологических особенностей терапевтического воздействия таблетированной формы цитофлавина, его эффективности и безопасности у детей с различными клиническими вариантами ППП ЦНС.
Материал и методы
Обследованы 176 детей дошкольного (5-6 лет) и раннего школьного (7-8 лет) возраста с различными клиническими вариантами ППП ЦНС: 35 детей с ДЦП, 47 детей с СНТ и 94 ребенка с ММД, 30 из которых вошли в группу контроля. Все группы были сопоставимы по полу и возрасту.
Оценка эффективности цитофлавина проводилась по данным неврологического осмотра, нейрофизиологического обследования, нейропсихофизиологического и речевого тестирования. Нейрофизиологическое обследование включало компьютерную электроэнцефалографию (ЭЭГ), транскраниальную допплерографию (ТКДГ) и компьютерную эхоэнцефалоскопию (Эхо-ЭС) с допплеровским исследованием ликвородинамики. Нейропсихофизиологическое тестирование проводилось с использованием компьютерного комплекса программ Spike-Children v. 2.7, включающих 24 стандартизированных теста, объединенных в 3 блока: нейропсихологический, психофизиологический и речевой. Исследование слухоречевой сферы у детей с СНТ осуществлялось с использованием оригинальной компьютерной программы Speech_Audiometry. Исследования проводились дважды: перед началом лечебно-реабилитационного курса и после его завершения. Пациенты наряду с физическими, физиотерапевтическими и психолого-педагогическими методами реабилитации получали монотерапию цитофлавином (ООО «НТФФ «Полисан», Санкт-Петербург, Россия) по схеме: 1 таблетка 2 раза в день (утром и в обед), ежедневно, на протяжении 25 дней. Всем детям с ММД, вошедшим в группу контроля и не получавшим медикаментозную терапию, проводили стандартный комплекс физических, физиотерапевтических и психолого-педагогических методов реабилитации. Было получено одобрение комитета по этике Иркутской государственной медицинской академии последипломного образования.
Для обработки результатов исследований применяли общепринятые методы вариационной статистики. Оценку достоверности статистических различий проводили параметрическими и непараметрическими методами с помощью критериев Стьюдента, Манна-Уитни, Уилкоксона. Различия считались статистически достоверными при уровне значимости не менее 95%. Расчеты производились на персональном компьютере при помощи пакета программ MS Excel 2010, Биостат, isica 6.0.
Результаты и обсуждение
Наиболее распространенными немоторными синдромами при ДЦП явились церебрастенический синдром (85%) и синдром ликвородинамических нарушений (65%), а также синдром вегетативной дистонии (65,2%). В неврологическом статусе детей с СНТ у 72,3% выявлялась рассеянная неврологическая симптоматика в виде оживления глубоких рефлексов, анизорефлексии, недостаточности мелкой моторики; у 65,9% детей наблюдались легкие и умеренные дискоординаторные нарушения. В рамках основного заболевания у всех детей встречалась вторичная задержка речевого развития различной степени выраженности, варианты детских дисфазий, проявления дислексии, дисграфии, реже дискалькулии. Признаки церебрастенического синдрома достоверно чаще (p<0,05) встречались среди детей раннего школьного возраста, что наиболее вероятно могло быть связано с недостаточной адаптацией к школьным нагрузкам.
Характерный для большинства детей с ММД синдром дефицита внимания и гиперактивности регистрировался у 22,9% детей с ДЦП, проявляясь неусидчивостью, недостатком активного внимания, повышенной утомляемостью во время занятий, истощаемостью при игровой деятельности, а также при проведении различных лечебно-реабилитационных мероприятий. При СНТ нарушения поведения отмечались у 80,6%, достоверно чаще (p<0,01) встречаясь в группах детей со средней и тяжелой степенями СНТ. Нарушения сна в виде трудностей засыпания, поверхностного, прерывистого сна и парасомний имелись 27,3% детей с ППП ЦНС. Частота эпилептического синдрома при ДЦП в среднем составила 13,5%, при СНТ коморбидность с эпилепсией отмечалась в единичных случаях, и только при ММД выявление эпилептогенных механизмов являлось критерием исключения из данной нозологической группы.
Комплексная нейропротективная терапия у детей с ППП ЦНС направлена на уменьшение выраженности двигательных нарушений, коррекцию эмоциональных и поведенческих расстройств, нормализацию уровня мозгового кровотока и ликвородинамики, улучшение обменных процессов в ткани мозга, а также стимулирование развития ВПФ. Так, на фоне лечения цитофлавином у детей с ДЦП достоверно (p<0,01) уменьшилась выраженность парезов: увеличился объем активных движений, снизилась спастичность мышечных групп. Было отмечено уменьшение дискоординаторных расстройств, достоверно (p<0,05) чаще имевших место у детей с двойной гемиплегией и атонически-астатической формой.
Большое значение у детей с ППП ЦНС имели количественная оценка состояния ВПФ в процессе реабилитации, составление нейропсихофизиологического профиля ребенка в динамике.
На фоне лечения цитофлавином отмечалось достоверное улучшение результатов нейропсихофизиологических тестов – повторения фраз, ритмов, вербальной слуховой памяти и минимальной скорости простой сенсомоторной реакции в группе детей с ДЦП (p<0,05). У детей с СНТ отмечено достоверное улучшение звукопроизношения и разборчивости речи, повышение концентрации и устойчивости внимания в теппинг-тесте, по данным сенсомоторных реакций выявлено улучшение средней скорости реакции, уменьшение количества ошибок (p<0,05). В группе детей с ММД было отмечено достоверное (p≤0,05) улучшение речи, праксиса, гнозиса, отчетливое повышение концентрации и устойчивости как поддерживаемого, так и избирательного внимания в сравнении с детьми контрольной группы, а также значимое (p<0,01) увеличение объема вербальной слуховой памяти.
При сравнении с возрастными нормативами в фоновой записи ЭЭГ у большинства детей с ППП ЦНС отмечалось усиление процессов синхронизации и преобладание мощности медленноволновой части спектра, что можно соотнести с ослаблением корковых влияний и доминированием неспецифических подкорковых структур. На фоне терапии цитофлавином при ММД было зафиксировано достоверное повышение индекса α-ритма – с 8,7±5,1 до 13,6±4,7, p<0,05; при СНТ – с 5,1±2,1 до 8,2±4,4, p<0,05; при ДЦП достоверное повышение индекса α-ритма наблюдалось только при двойной гемиплегии (с 2,2±2,4 до 6±4,5, p<0,05). Таким образом, в целом у детей с ППП ЦНС отмечалась устойчивая тенденция к снижению количества и амплитуды Δ-колебаний, повышению индекса α-ритма.
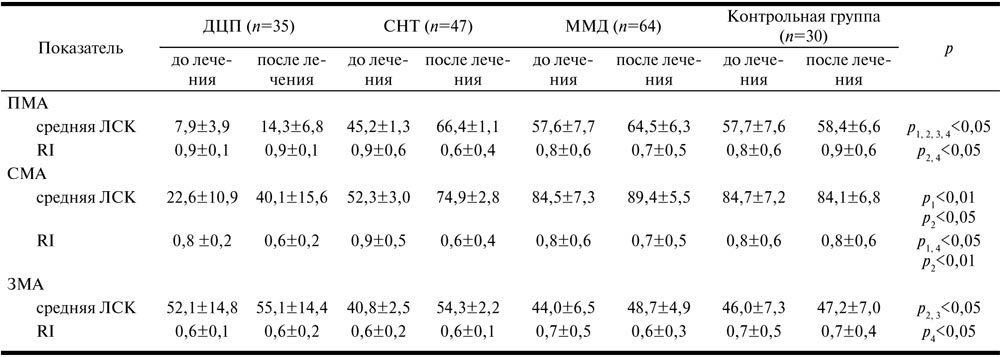
Анализ уровня мозгового кровотока у детей с ДЦП до лечения цитофлавином выявил значительное его снижение в передних отделах головного мозга. Например, средняя линейная скорость кровотока (ЛСК) в русле передней мозговой артерии (ПМА) при различных формах ДЦП в среднем составила 7,9±3,9 см/с при возрастной норме 71±5 см/с [12]; средняя ЛСК в русле средней мозговой артерии (СМА) составила 22,6±10,9 см/с при норме 97±9 см/с; при этом в задней мозговой артерии (ЗМА) кровоток был снижен в меньшей степени, а в некоторых случаях был нормальным и даже повышенным (см. таблицу). Сохранность кровотока, а иногда его повышение в вертебрально-базилярной системе у детей со спастическими формами ДЦП можно расценивать как механизм компенсации выраженной гипоперфузии в каротидном бассейне. В норме средняя ЛСК в русле ЗМА равна 57±9 см/с [12] (см. таблицу).
Сравнительные данные ТКДГ у детей с ППП ЦНС до и после лечения цитофлавином (M±m)

Примечание. p1 – различия в группе детей с ДЦП до и после лечения цитофлавином; p2 – различия в группе детей с СНТ до и после лечения цитофлавином; p3 – различия в группе детей с ММД до и после лечения цитофлавином; p4 – различия в группе детей с ММД в сравнении с группой контроля.
Существенную роль в формировании и персистировании механизмов церебральной гипоперфузии у детей с ППП ЦНС играют вазоспастические реакции в микроциркуляторном русле. Так, у детей с ДЦП индекс Пурсело (RI), отражающий тонус сосудов и периферическое сосудистое сопротивление, в каротидном бассейне был значительно повышен (0,8±0,2-0,9±0,1 при норме 0,5-0,7), а в русле ЗМА RI был в пределах нормы (0,6±0,1).
У большинства детей с СНТ выявлено умеренное диффузное снижение церебрального кровотока (в среднем на 30-40% от возрастных нормативов), при этом обращало внимание существенное повышение RI в каротидном бассейне, однако в русле ЗМА гипоперфузия нередко сочеталась с нормальными показателями RI (0,6±0,2).
При ММД достоверное (p<0,05) негрубое снижение церебрального кровотока (в среднем на 20-25% от возрастных нормативов) отмечалось в русле ПМА и ЗМА при достаточно сохранных показателях кровотока в русле СМА. Как и при других формах ППП ЦНС, при ММД наблюдалась тенденция к повышению сосудистого тонуса в каротидном бассейне, но достоверно в меньшей степени (RI=0,8±0,6, p<0,05).
На фоне лечения цитофлавином во всех исследуемых группах достоверно нарастала средняя ЛСК (p<0,05), преимущественно в каротидном бассейне (см. таблицу). Так, средняя ЛСК максимально повысилась в группах детей с ДЦП и СНТ (в каротидном бассейне – на 80-85 и 40-45% соответственно), тогда как в группе детей с ММД данное повышение составило только 5-15% от исходных значений. Уменьшение признаков гипоперфузии, как правило, сопровождалось снижением либо нормализацией RI. Увеличение средней ЛСК в русле ЗМА было достоверным только в группах детей с СНТ и ММД (p<0,05), при этом препарат не оказывал существенного влияния на исходно нормальные показатели RI.
Таким образом, у детей дошкольного и младшего школьного возраста с ППП ЦНС цитофлавин оказывает нормализующее действие на основные показатели церебральной гемодинамики, главным образом за счет уменьшения вазоспастических реакций и повышения уровня мозгового кровотока, в большей степени – в каротидном бассейне. К основным преимуществам применения цитофлавина у детей с ППП ЦНС можно отнести нормализующее влияние на церебральный кровоток, а также на отчетливое ноотропное и противоастеническое действия. Учитывая простоту применения препарата, доказанную клиническую эффективность и безопасность, таблетированная форма цитофлавина может быть рекомендована для курсовой терапии детей дошкольного и младшего школьного возраста с ППП ЦНС.
Конфликт интересов отсутствует.
Литература
- Детская неврология. Клинические рекомендации. Под ред. В.И. Гузевой. М.: МК; 2014.
- Немкова С.А. Детский церебральный паралич: диагностика и коррекция когнитивных нарушений. М.: Союз педиатров России; 2012.
- Скворцов И.А. Неврология развития. М.: Литтерра; 2008.
- Классификация перинатальных поражений нервной системы и их последствий у детей первого года жизни. Методические рекомендации. Под ред. Н.Н. Володина. М.: ВУНМЦ; 2006.
- Пальчик А.Б., Шабалов Н.П. Гипоксически-ишемическая энцефалопатия новорожденных. М.: МЕДпресс-информ; 2006.
- Петрухин А.С. Неврология детского возраста. М.: Медицина; 2004.
- Volpe J. Neurology of Newborn. NY.: Ch. L.; 2002.
- Breneman AI, Gifford RH, Dejong MD. Cochlear Implantation in Children with Auditory Neuropathy Spectrum Disorder: Long Term Outcomes. Journal of the American Academy of Audiology. 2012;23(1):5-17.
doi: 10.3766/jaaa.23.1.2
- Zavadenko NN, Simashkova NV. New Approaches to the Diagnosis of Attention Deficit Hyperactivity Disorder. Neuroscience and Behavioral Physiology. 2015;45(7):837-842.
doi: 10.1007/s11055-015-0152-2
- Bhutta AT, Cleves MA, Casey PH, Cradock MM, Anand KJS. Cognitive and behavioral outcomes of school-aged children who were born preterm: a -analysis. JAMA. 2002;288(6):728.
doi: 10.1001/jama.288.6.728
- Fraello D, Maller-Kesselman J, Vohr B, Katz KH, Kesler S, Schneider K, Reiss A, Ment L, Spann MN. Consequence of preterm birth in early adolescence: the role of language on auditory short-term memory. J Child Neurol. 2011;26(6):738-742.
doi: 10.1177/0883073810391904
- Никитин Ю.М., Труханов А.И. Ультразвуковая допплерографическая диагностика сосудистых заболеваний. М.: Видар; 1998.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
Повышение эффективности медицинской помощи детям разного возраста, в том числе и самого младшего, представляет собой одну из наиболее актуальных медико-социальных задач. Особого внимания в области неонатальной и педиатрической патологии требуют гипоксически-ишемические и инфекционные поражения ЦНC. Проблемы перинатальной патологии актуальны как в связи с их высокой частотой среди заболеваний новорожденных и детей первого года жизни (по данным ряда авторов, от 60% до 80% с тенденцией к дальнейшему росту), так и из-за наличия нерешенных вопросов диагностики и терапии. К этому следует добавить, что перинатальные поражения ЦНС способствуют развитию ранней психоневрологической инвалидизации (ранняя инвалидность среди детей встречается в 60-70% случаев) [1-4].
Гипоксически-ишемические поражения ЦНС
Одним из наиболее значимых патогенетических факторов перинатальных повреждений ЦНС новорожденных является гипоксия. Гипоксия плода, часто развивающаяся вследствие патологического протекания беременности, способствует появлению на свет недоношенного ребенка с нарушением дыхательной функции. Недоношенные, и особенно глубоко недоношенные, дети отличаются выраженными физиологическими отклонениями. К их числу относятся гиперкатехоламинемия, карнитиновая недостаточность, рассыпной тип коронарных артерий, что в свою очередь приводит к значительному ингибированию синтеза макроэргов в митохондриях кардиомиоцитов и преобладанию углеводного компонента обмена, в результате чего запускает каскад патобиохимических и патобиологических нарушений. Все это приводит к формированию респираторного ацидоза с вторичным развитием тканевой гипоксии и метаболического ацидоза. Гиперкатехоламинемия способствует стимуляции сосудодвигательного центра и сердечной деятельности, повышению тонуса артериол и гипертензии, приводя в дальнейшем к аритмии, снижению чувствительности адреналовых рецепторов и в конечном итоге – к выраженной сердечной недостаточности. В итоге у глубоко недоношенных детей утрачивается способность адекватно отвечать на послеродовую перестройку кровообращения, что в свою очередь приводит к выраженному функциональному напряжению сердечно-сосудистой системы.
Как известно, кровообращение плода имеет особенности, заключающиеся прежде всего в том, что легкие не осуществляют дыхательную функцию, в связи с чем не функционирует малый круг кровообращения, при этом кислород поступает из плаценты по пупочной вене и проходит по нижней полой вене в правое предсердие. Для того чтобы насыщенная кислородом кровь могла попасть в большой круг кровообращения, у плода функционируют основные фетальные протоки: аранциев проток между пупочной веной и нижней полой веной, соединяющий правое и левое предсердия, и артериальный проток между аортой и легочным стволом. После рождения в норме они должны закрыться, чего у глубоко недоношенных детей часто не происходит.
Следствием метаболического ацидоза является усугубление нарушения кровообращения во всех тканях организма, в том числе нарушение кровообращения тканей головного мозга. Возникающая нестабильность ауторегуляции кровотока головного мозга в связи с морфофункциональной незрелостью основных ее компонентов сопровождается высокой частотой ишемических и геморрагических поражений головного мозга новорожденных, которые в свою очередь ведут к тем или иным разной степени выраженности отклонениям в нервно-психическом развитии и ранней детской инвалидизации.
Согласно данным ряда авторов [4-7], 85% всех перинатальных поражений ЦНС у недоношенных детей проявляются в течение первой недели их жизни.
Анализ патофизиологических механизмов постгипоксического поражения головного мозга недоношенных детей обусловил понимание необходимости его ранней фармакологической коррекции. Такая коррекция призвана предотвратить или по крайне мере в значительной мере уменьшить выраженность повреждений головного мозга, повысить терапевтический и реабилитационный потенциал и улучшить прогноз заболевания [4, 8-10].
При рассмотрении проблемы ранней фармакологической коррекции следует иметь в виду, что существуют расхождения взглядов на продолжительность так называемого «терапевтического окна», в рамках которого фармакологическая нейроцитопротективная коррекция при гипоксических и ишемических нарушениях может быть признана эффективной. В литературе [7, 10] можно встретить следующий диапазон данного «терапевтического окна» – от 2 до 48 ч после развития гипоксически-ишемических нарушений. Подобные рамки «терапевтического окна» связаны с постулатом, что наиболее значительные клеточные потери нервной ткани развиваются спустя 2, 6 и 48 ч после рождения ребенка вследствие оксидантного стресса, который сопровождает реперфузию головного мозга, когда фаза дефицита перфузии переходит в фазу реперфузии высокооксигенированной кровью, что в свою очередь сопровождается избыточной продукцией высокореакционных свободных радикалов или продуктов, их генерирующих [11]. В подобной ситуации в первые часы и сутки жизни детей, перенесших анте- и интранатальную гипоксию и ишемию, возникает выраженный дисбаланс регуляции и распределения мозгового кровообращения, что способствует, особенно у недоношенных детей, частому развитию ишемических и геморрагических нарушений тканей головного мозга в раннем неонатальном периоде [4, 12].
Наиболее перспективными направлениями медикаментозной коррекции гипоксических и ишемических поражений структур головного мозга как у взрослых, так и у детей в настоящее время рассматривается [7, 13] использование регулирующих внутриклеточный метаболизм антигипоксантов, в состав которых входят естественные метаболиты, которые в то же время активизируют продукцию макроэргов в условиях дефицита кислорода и обладают антиоксидантной активностью [14].
К отвечающим указанным требованиям лекарственным средствам можно с уверенностью отнести препарат цитофлавин (ООО «НТФФ «ПОЛИСАН», Санкт-Петербург). Данный препарат является одним из немногих нейроцитопротекторов, эффективность и безопасность которого были оценены с позиций доказательной медицины.
Цитофлавин оказывает нейроцитопротективное, антигипоксическое, антиоксидантное действие, положительно влияя на процессы энергообразования в клетке, уменьшая продукцию свободных радикалов и восстанавливая активность ферментов антиоксидантной защиты [15]. Так, в биофармацевтических исследованиях [16, 17] было установлено, что цитофлавин улучшает окислительный метаболизм в условиях ишемии, препятствуя резкому снижению уровня АТФ, стимулирует активность аденилатциклазы, что позволяет осуществлять анаэробный метаболизм глюкозы без образования лактата. Данный препарат стимулирует также репаративные процессы и ограничивает зону ишемического повреждения [18]. Кроме того, цитофлавин улучшает оксигенацию крови и активизирует клеточное дыхание, а также транспорт ионов и синтез белков. Препарат, сохраняя аппарат рибосом, активирует внутриклеточный синтез нуклеиновых кислот, ферментативные процессы цикла Кребса, способствует утилизации глюкозы и синтезу и внутриклеточному накоплению АТФ и других макроэргов [19]. Важно также, что при терапии пациентов с гипоксией и ишемией головного мозга цитофлавин способствует ресинтезу γ-аминомасляной кислоты в нейронах [20, 21].
Цитофлавин представляет собой гармоничную комбинацию янтарной кислоты, рибоксина, никотинамида (витамин РР) и рибофлавина мононуклеотида (витамин В2). Янтарная кислота является центральным субстратом цикла Кребса и может включаться в данный цикл в ионизированной форме, преодолевая клеточные и митохондриальные мембраны. Рибоксин способствует ингибированию фермента ксантаноксидазы и подавлению свободнорадикальных процессов, тем самым обеспечивая антиоксидантное действие. Рибофлавин, являющийся профактором основных коферментов дыхательной цепи флавинмононуклеотида и флавинадениндинуклеотида, обладает прямым антигипоксическим действием, которое связано с активированием флавинредуктаз и восстановлением уровня АТФ, а также антиоксидантными свойствами, обусловленными восстановлением глутатиона. Никотинамид активирует антиоксидантные системы убихиноновых оксиредуктаз, которые оказывают защитное действие в отношении клеточных мембран.
Таким образом, все компоненты цитофлавина являются индукторами клеточных метаболических путей и активаторами процессов образования энергии, что в свою очередь способствует утилизации свободного кислорода и соответственно снижает уровень перекисных процессов. Немаловажным преимуществом данного препарата является наличие в его составе метилглюкамина – трансмембранного переносчика, который переносит связанные с ним соединения через клеточные мембраны во внутренние структуры клетки, где и происходят все основные патохимические нарушения при гипоксии и ишемии.
Необходимо отметить, что важную роль в развитии и созревании структур детского головного мозга играют тиреоидные гормоны. Неонатальный транзиторный гипотиреоз оказывает неблагоприятное влияние на развитие детей (физическое, речевое, психическое), а также на уровень их социальной адаптации [22, 23]. В свою очередь основными патогенетическими механизмами развития перинатальных поражений как нервной системы, так и щитовидной железы являются гипоксия и соответственно недостаточная тканевая перфузия, что способствует нарастанию энергетического дефицита и нарушению внутриклеточного гомеостаза. Учитывая описанные выше нарушения, становится понятным важность применения при перинатальных поражениях ЦНС и щитовидной железы антигипоксантов, обладающих мембраностабилизирующим действием [7, 10], к которым может быть отнесен и цитофлавин. Его эффективность была установлена в ряде исследований.
В исследовании В.И. Струкова и соавт. [24] анализировалась эффективность базовой терапии и терапии с включением в схему лечения детей в возрасте от 7 сут до 1 мес, родившихся при сроке беременности от 37 до 42 нед и страдающих ишемией головного мозга и транзиторным гипотиреозом, цитофлавина. В группе пациентов, получавших цитофлавин, на 5-6-е сутки терапии наблюдалось статистически значимое уменьшение степени выраженности ишемии тканей головного мозга по сравнению с группой пациентов, не получавших цитофлавин. Также было выявлено статистически значимое более быстрое снижение уровня ТТГ в сыворотке крови пациентов, лечившихся цитофлавином. Результаты проведенного исследования показали также эффективность цитофлавина при терапии детей с экстремально низкой и очень низкой массой тела с постгипоксическими повреждениями миокарада и значительными нарушениями метаболизма. У них отмечалась нормализация показателей кислотно-щелочного равновесия в течение суток от начала лечения без повышения риска развития внутрижелудочковых кровоизлияний. Анализируя среднюю продолжительность симптомов перинатального поражения ЦНС, авторы исследования пришли к выводу о значительно меньшей их продолжительности (в 1,5-2 раза) в группе получавших цитофлавин больных. К таким симптомам относили нарушение двигательной активности, вегетовисцеральную дисфункцию, расстройство сна, снижение аппетита и нарушение прибавки массы тела.
Интересными и полезными с практической точки зрения оказались результаты исследования, проведенного С.О. Рогаткиным и соавт. [25], которые изучали эффективность цитофлавина при постгипоксических поражениях ЦНС у недоношенных новорожденных. Было подтверждено церебропротективное действие данного препарата. Так, среди новорожденных, получавших цитофлавин, по сравнению с теми, кто не получал данный препарат, был выявлен статистически значимый уровень снижения частоты развития и тяжести ишемических и геморрагических поражений ЦНС. Этому соответствовал более низкий уровень концентрации нейроспецифических белков в крови, что в первую очередь связано с более быстрой нормализацией показателей кислотно-щелочного равновесия, парциального давления кислорода и углекислого газа, а также устранением лактат-ацидоза.
Благоприятное действие цитофлавина при ишемии головного мозга у недоношенных новорожденных установили также А.Г. Антонов и соавт. [26]. Ими было констатировано, что при применении цитофлавина происходило более быстрое и полное психомоторное развитие детей в течение первого года жизни.
Важно отметить, что, по результатам приведенных исследований, цитофлавин хорошо переносился детьми и у них отсутствовали побочные явления.
Таким образом, данные ряда исследований убедительно демонстрируют нейро- (церебро-)протективное действие цитофлавина при терапии детей с гипоксическими и ишемическими поражениями ЦНС, а также кардио- и тиреопротективное действие данного препарата у обсуждаемой категории пациентов, что, безусловно, дает основание для его использования для лечения детей первых месяцев жизни с расстройствами нейрометаболизма в рамках комплексного лечения перинатальных поражений ЦНС.
Инфекционные поражения ЦНС
Известно, что инфекционные поражения ЦНС занимают одно из ведущих мест среди всех инфекционных заболеваний. Они отличаются тяжелым течением и высоким уровнем летальности (8-36%). Частота остаточного поражения нервной системы составляет 26-75% [27]. Признаки и проявления стойкого органического поражения ЦНС в резидуальном периоде отмечаются практически у 50% детей, перенесших инфекционное поражение нервной системы [27], в связи с чем повышение эффективности терапии детей с инфекционными заболеваниями, и прежде всего с бактериальными гнойными менингитами и вирусными энцефалитами, является одной из наиболее актуальных медико-социальных проблем.
Одним из основных проявлений инфекционных процессов в ЦНС является поражение сосудистого русла и нарушение системы гемостаза. Сосудистые поражения, развивающиеся на фоне инфекционных заболеваний, включают в себя окклюзию и стенозы сосудов, развитие которых в свою очередь связано с нарушением реологических свойств крови. При инфекционных поражениях ЦНС наиболее часто встречается генерализованное поражение сосудов, вовлекающее в патологический процесс сосуды головного мозга. Их поражение характеризуется повреждением эндотелия, нарушением нейрососудистой регуляции и коагуляции, что диктует необходимость своевременного применения различных вазоактивных и нейроцитопротективных препаратов.
При лечении инфекционной патологии в педиатрии предпочтение отдается комплексным препаратам [27], обладающим мультимодальным и многофакторным действием, каковым является и рассматриваемый в данной статье цитофлавин. Он был объектом изучения в ряде работ.
Н.В. Скрипченко и Е.С. Егорова [27] оценивали эффективность терапии пациентов в возрасте от 1 мес до 18 лет, перенесших бактериальный гнойный менингит и вирусный энцефалит. Все пациенты получали стандартную терапию (антибактериальные или противовирусные препараты и дегидратационные средства) и были разделены на две группы – получавшие и не получавшие цитофлавин на фоне базовой терапии. Авторами был сделан вывод, что применение цитофлавина в течение острого периода бактериального гнойного менингита и вирусного энцефалита способствует сокращению длительности основных клинических симптомов заболевания. Авторы эти изменения связали с мультимодальным и многофакторным действием данного препарата, а именно со способностью цитофлавина благоприятно влиять как на улучшение кровообращения головного мозга, так и на стимуляцию и активизацию нейрометаболических процессов. Кроме того, результаты рассматриваемого исследования свидетельствовали о нормализации под влиянием цитофлавина клинических показателей крови и противовоспалительном действии данного препарата. Было высказано предположение [18, 28], что это связано с активацией метаболических процессов и ингибирования синтеза провоспалительных цитокинов. Кроме того, применение цитофлавина способствовало быстрой нормализации показателей циркулирующих эндотелиоцитов и D-димера. Было отмечено также благоприятное влияние цитофлавина на реологические свойства крови.
Таким образом, применение препарата цитофлавин у детей в качестве патогенетической терапии в острой стадии бактериального гнойного менингита и вирусного энцефалита является эффективным. Кроме того, установлены хорошая переносимость и безопасность цитофлавина. Цитофлавин не только оказывает противовоспалительное и нейропротективное действие, но и улучшает реологические свойства крови. Благодаря совершенствованию лечения пациентов детского возраста, перенесших бактериальный гнойный менингит и вирусный энцефалит, с помощью цитофлавина были достигнуты снижение среднего койко-дня, а также значительное уменьшение риска возникновения резидуального неврологического дефицита – с 35 до 15%.
Сказанное выше повышает возможность терапии поражений ЦНС гипоксически-ишемической и инфекционной этиологии. Следует подчеркнуть, что эффективность данной терапии зависит от комплексного комбинированного и многофакторного подхода к ее проведению. Из представленного обзора литературы видно, что проведение протекции в настоящее время возможно с помощью своевременного назначения энергокорригирующего антиоксиданта и антигипоксанта цитофлавина, применение которого при терапии данной категории пациентов является оправданным с точки зрения эффективности и безопасности и может быть рекомендовано для использования в практической неонатологии и педиатрии.
Авторы заявляют об отсутствии конфликта интересов.
*: vikoval67@mail.ru; https://orcid.org/0000-0002-1004-2162
Источник
